江苏齐氏生物科技有限公司品牌商
16 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
推荐产品
技术资料/正文
代谢π析(二)——底物消耗慢,产物反而多?
53 人阅读发布时间:2026-01-26 16:33
引言
数据出现看似矛盾的裂缝,往往是新发现的起点。
在上一期的 《代谢π析》 中,我们通过维拉帕米(Verapamil)的案例,揭示了“低效通路劫持”这一反常现象。今天,我们把目光投向案例中的另一个主角——Midazolam。它的数据呈现出一个更精妙,也更值得玩味的“矛盾”,而这个矛盾将我们引向代谢研究更深的层面。
01 重现谜题:一个“矛盾”的数据点
让我们回顾一下上期的核心数据(基于肝S9代谢稳定性实验):
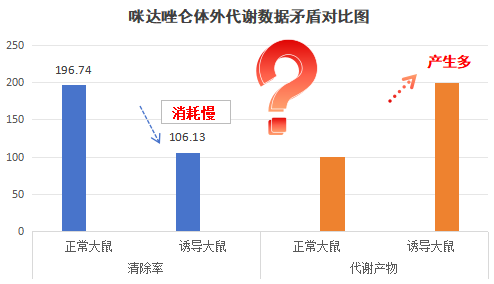
数据显示,在PB/BNF诱导的大鼠S9中,Midazolam的固有清除率明显更低(意味着它从体系中“消失”得更慢)。这与“酶诱导会加速代谢”的直观预期相悖。
然而,当我们进一步分析孵育体系时,可能会发现另一个现象:在诱导S9中,Midazolam的某个特定代谢物(例如其主要的1-羟基代谢物)的生成量,反而比在正常S9中更高。
这就构成了一个核心矛盾:为什么诱导S9“吃”底物吃得慢,但“吐”出某个特定产物却更多?
02 一个假设:是否存在“不成熟”的酶?
面对这个矛盾,一个大胆而富有洞察力的猜想被提出来:在非诱导的正常S9中,部分CYP3A酶蛋白是否可能处于“不成熟”状态?
· 假说推演:正常生理状态下,肝脏持续合成各种酶蛋白。部分新合成的CYP3A可能尚未完成正确的折叠、血红素辅基的嵌入等翻译后成熟过程。这些“半成品”酶也许能结合Midazolam,并启动代谢反应,但无法高效地将底物全部转化为最终可检测的稳定产物,可能停滞在某个不稳定的中间体状态。
· 假说推论:这能解释为何正常S9消耗底物快(很多“半成品酶”在消耗底物),但特定终产物的产率却偏低(反应未完成)。反之,诱导过程可能促进了CYP3A的成熟,使每个功能酶分子都能“善始善终”,高效产出可检测的代谢物。
这是一个具有启发性的思路,它将我们的关注点从单纯的“酶数量”拓展到了“酶质量”与“功能完整性”的层面。 然而,科学需要验证。
03 更可能的解释路径:代谢网络的动力学重塑
在诉诸“不成熟酶”这一相对复杂的假说前,我们通常优先考虑用经典的药代动力学原理和更直接的实验证据来解释。以下是对该现象更主流的几种解释方向:
方向一:代谢物谱的“转向”
这是最可能的原因。CYP3A代谢Midazolam并非只产生一种代谢物,其主要途径包括生成1-羟基Midazolam和4-羟基Midazolam。诱导处理可能改变了酶的特性,使其催化偏好发生“转向”。
打个比方:正常S9像一座同时生产A、B两种产品的小工厂,总量有限;诱导S9则像一座经过升级、专门优化了A产品生产线的大工厂。虽然大工厂的原料吞吐总速度(对应总清除率)可能因为管理复杂而稍慢,但其A产品的产线效率(对应特定代谢物生成速率)却可以非常高。
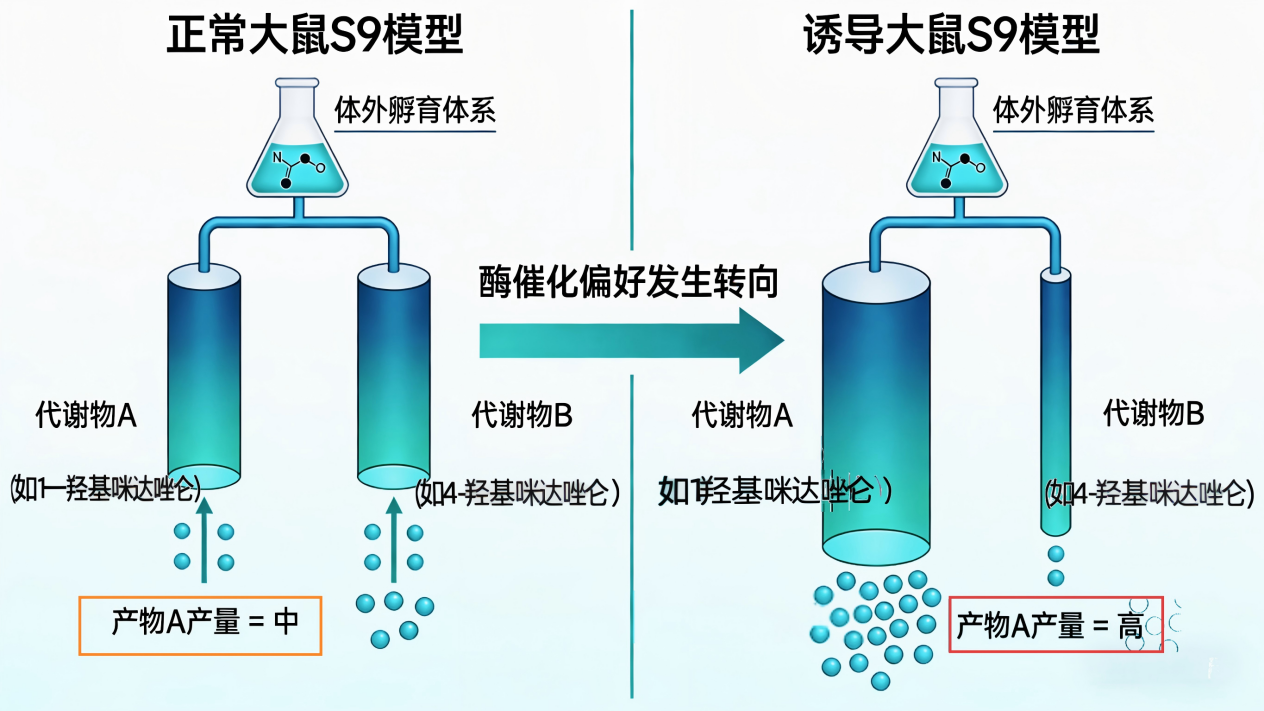
如上图所示,诱导处理可能改变了CYP3A的催化“偏好”,使其从均衡生产多种代谢物,转向高度集中于生产我们正在检测的那一种特定代谢物(如1-羟基Midazolam)。这解释了为何在总清除率下降的情况下,该特定产物的生成量反而更高——因为酶工厂的“生产线”被重新优化了。
验证方法:进行代谢物鉴定分析,使用高分辨质谱全景式对比两种S9中产生的所有代谢物种类和相对丰度。
方向二:酶动力学的“效率陷阱”
底物消耗速度(CLint)反映的是代谢的整体清除率,而单个代谢物的生成速率则受限于其特定的催化步骤。诱导后,虽然CYP3A总量大增,但其催化效率(如Vmax/Km) 可能并未同比提升,甚至可能因体系内竞争而改变。
验证方法:分别测定两种S9中CYP3A对Midazolam代谢的酶动力学参数,比较其实际催化效率。
方向三:下游反应的“加速清空”
诱导可能同时上调了后续代谢酶(如负责将羟基化代谢物进行葡糖醛酸化的UGT酶)的活性。在诱导S9中,初级代谢物被迅速转化为次级代谢物,从而在检测初级产物的时间点上,其表观积累量可能更低;而非诱导S9中,初级产物因转化慢而积累更多。
验证方法:在孵育体系中加入UGT酶的共因子(UDPGA),或使用广谱的UGT抑制剂,观察初级代谢物积累量的变化。
04 从猜想到实证:设计您的验证方案
面对复杂的矛盾数据,系统性地验证是通往真相的路径。下图展示了一个从现象到本质的经典研究闭环:
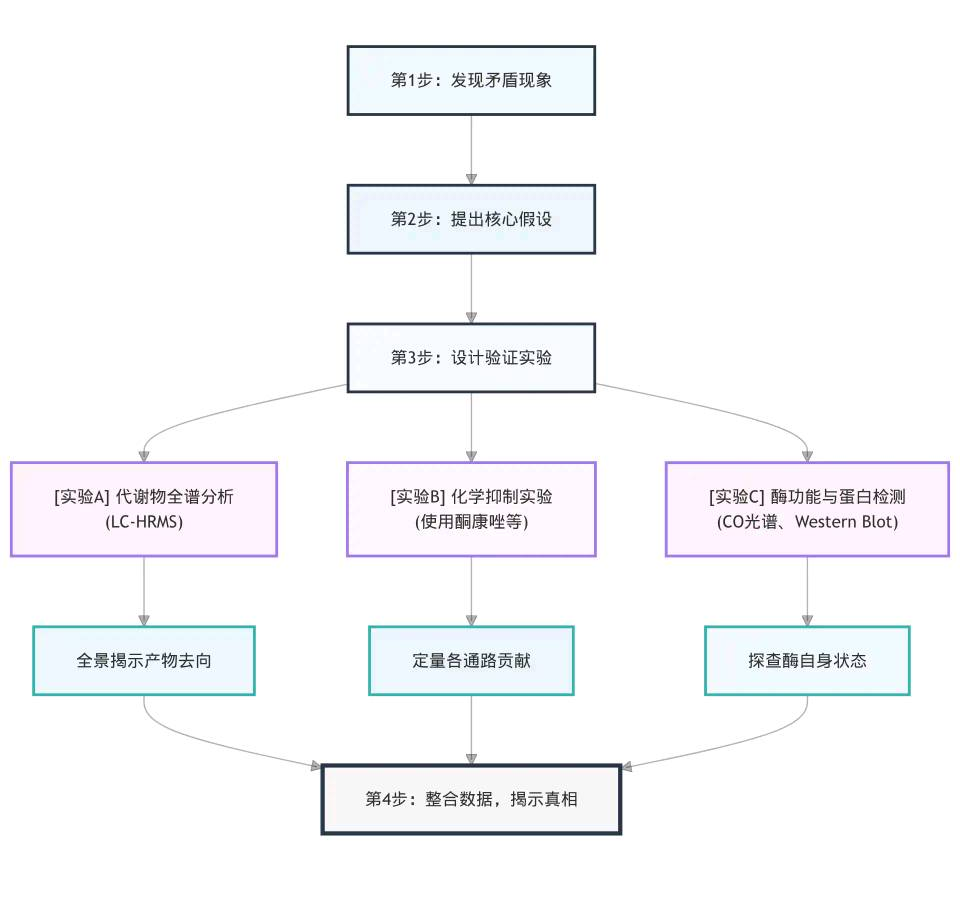
遵循这一逻辑,我们可以层层深入地设计实验,下表则提供了具体的实验方案与目标:
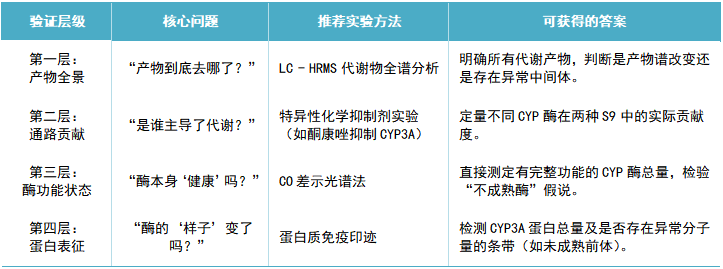
05 结语:矛盾是进步的阶梯
Midazolam的这个案例告诉我们,体外代谢数据绝非简单的数字比较。一个看似“矛盾”的数据点,背后可能隐藏着代谢通路的转向、酶动力学的深层次信息,甚至是关于酶蛋白自身生物发生的奥秘。

面对这样的数据,我们应当:
1. 拥抱矛盾:将其视为深入探索的契机,而非需要“抹平”的误差。
2. 建立假设:基于机制提出合理的猜想(如本文的“不成熟酶”假说)。
3. 系统验证:设计层层递进的实验,揭开真相。
这,正是体外代谢研究的魅力所在,也是高质量、特性明确的肝S9等研究工具价值凸显之处——只有从源头保证实验体系的可靠与稳定,我们才能自信地将数据差异归因于生物学机制,而非试剂本身的波动。
(本文由 [齐氏生物] 提供技术支持。我们不仅提供高质量的诱导/非诱导肝S9等关键试剂,更致力于与客户一同破解数据背后的代谢密码,为精准研发提供坚实基石。)